クロフィブラート軟膏のパイロットスタディ・説明と同意書
※表題の「パイロットスタディ」は当初「小規模治験」となっていました。「治験という語は製薬会社が厚労省に流通薬としての認可を求める際の用語なのでふさわしくない」という指摘があり、もっともなことなので修正しました。ただし患者向け説明と同意書中の字句はあとから変更すべきではないのでそのままになっています。
先日掲示した、クロフィブラート軟膏についてのパイロットスタディですが、協力していただける担当医の先生がなかなか見つからないので、ブラインドテストにする方法を少し工夫したうえで、わたしが自分で診察して効果を確認することにしました。患者からの直接申込みを受け付けます。
20人を予定しています。<被験者となるための条件>をよく確認した上で、参加頂けるかたはFAXしてください。お待ちしています。
(注:試験は終了しました。ご協力ありがとうございました。)
追記1)
予備試験というほどでもないのですが、この「クロフィブラート軟膏」、私が自分自身の健常皮膚に2週間連日外用した限りでは、一次刺激もなく(かぶれなかったということ)使用感に問題はありませんでした。
理論上、ペリオスチンを介する「アトピー慢性化」の輪を断ち切りますし(→こちら)、動物実験でもステロイド外用後のリバウンドを抑えます(→こちら)。
ステロイド離脱後、リバウンドが遷延してなかなか治まらない方に向いているのではないかと思われます(わたしの関心もまた、まさにそこを確認したいの一点にあります)。
追記2)
年齢を「15ー30才」から「15才以上」に変更しました。
下記と同じものがpdfファイルでUPしてあります(→こちら)。ダウンロードの上、印刷して御使用ください。
ーーーーー(ここから)-----
クロフィブラート軟膏の治験についての説明と同意書
クロフィブラートは、高脂血症のお薬で、日本で内服薬として普通に外来で処方されているものです。
クロフィブラートと作用機序の同じ薬剤 (PPARαアゴニスト)を添加した軟膏が、ステロイド外用剤を使用していないアトピー性皮膚炎の皮疹や、ステロイド外用剤中止後のリバウンドを、軽減することが、マウスを用いた動物実験において示されています(1)(2)。
今回、クロフィブラートの臨床効果を確認する目的で、白色ワセリンを軟膏基剤として「クロフィブラート軟膏(0.25%)」を調整し、ステロイドを外用していない患者において、その効果を確認する目的で、小規模の治験を企画しました。
予想される効果は、湿疹・皮膚炎の改善、およびアトピー性皮膚炎の病勢の血中マーカーであるTARC値の低下です。
起こりうる有害事象としては、接触皮膚炎(かぶれ)です。軟膏に添加されるクロフィブラートは、内服に比べて非常に微量なので(軟膏100gに対しクロフィブラート1錠です)、血中濃度の上昇は起こりえませんから、安全性は高いといえます。ただし、そうは言っても、予期しなかった有害事象が起こる可能性をまったく否定はできません。この点は十分御了解のうえ、治験にご参加ください。
<方法について>
1)患者(あるいは保護者のかた)と、医師双方から、皮膚炎の評価を行います。 今回はVASスケールというものを用います。
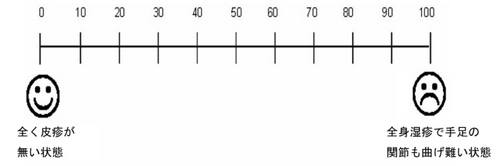
考えられるもっともよい状態を(まったく皮疹の無い状態)0、最も悪い状態(全身湿疹で関節も曲げ難いような状態)を100としたとき、現在の状態がいくつにあたるかを、下のVASスケールを見て指差して、数字を記録します。
先日掲示した、クロフィブラート軟膏についてのパイロットスタディですが、協力していただける担当医の先生がなかなか見つからないので、ブラインドテストにする方法を少し工夫したうえで、わたしが自分で診察して効果を確認することにしました。患者からの直接申込みを受け付けます。
20人を予定しています。<被験者となるための条件>をよく確認した上で、参加頂けるかたはFAXしてください。お待ちしています。
(注:試験は終了しました。ご協力ありがとうございました。)
追記1)
予備試験というほどでもないのですが、この「クロフィブラート軟膏」、私が自分自身の健常皮膚に2週間連日外用した限りでは、一次刺激もなく(かぶれなかったということ)使用感に問題はありませんでした。
理論上、ペリオスチンを介する「アトピー慢性化」の輪を断ち切りますし(→こちら)、動物実験でもステロイド外用後のリバウンドを抑えます(→こちら)。
ステロイド離脱後、リバウンドが遷延してなかなか治まらない方に向いているのではないかと思われます(わたしの関心もまた、まさにそこを確認したいの一点にあります)。
追記2)
年齢を「15ー30才」から「15才以上」に変更しました。
下記と同じものがpdfファイルでUPしてあります(→こちら)。ダウンロードの上、印刷して御使用ください。
ーーーーー(ここから)-----
クロフィブラート軟膏の治験についての説明と同意書
クロフィブラートは、高脂血症のお薬で、日本で内服薬として普通に外来で処方されているものです。
クロフィブラートと作用機序の同じ薬剤 (PPARαアゴニスト)を添加した軟膏が、ステロイド外用剤を使用していないアトピー性皮膚炎の皮疹や、ステロイド外用剤中止後のリバウンドを、軽減することが、マウスを用いた動物実験において示されています(1)(2)。
今回、クロフィブラートの臨床効果を確認する目的で、白色ワセリンを軟膏基剤として「クロフィブラート軟膏(0.25%)」を調整し、ステロイドを外用していない患者において、その効果を確認する目的で、小規模の治験を企画しました。
予想される効果は、湿疹・皮膚炎の改善、およびアトピー性皮膚炎の病勢の血中マーカーであるTARC値の低下です。
起こりうる有害事象としては、接触皮膚炎(かぶれ)です。軟膏に添加されるクロフィブラートは、内服に比べて非常に微量なので(軟膏100gに対しクロフィブラート1錠です)、血中濃度の上昇は起こりえませんから、安全性は高いといえます。ただし、そうは言っても、予期しなかった有害事象が起こる可能性をまったく否定はできません。この点は十分御了解のうえ、治験にご参加ください。
<方法について>
1)患者(あるいは保護者のかた)と、医師双方から、皮膚炎の評価を行います。 今回はVASスケールというものを用います。
考えられるもっともよい状態を(まったく皮疹の無い状態)0、最も悪い状態(全身湿疹で関節も曲げ難いような状態)を100としたとき、現在の状態がいくつにあたるかを、下のVASスケールを見て指差して、数字を記録します。
2)皮疹部の写真撮影をします。写真は個人が特定されないように配慮したうえで(たとえば、体の皮疹が主体であれば、顔は除く、顔の皮疹が主体であれば、眼周りをマスクする、など)、学会報告や医学論文の投稿の際に使用します。
3)血液検査をします。TARCというアトピー性皮膚炎の病勢の指標となる検査項目です。
4)担当医から処方された軟膏(※注)を外用します。1日1回、皮膚炎の個所にFTU(フィンガーチップユニット)の考えに準じて外用します。すなわち、大人の人差し指先端から第一関節までの一すくい分を、大人の手のひら二つ分くらいの面積に外用します。これを2週間続けてください。ただし、かぶれなど、肌に合わない兆候が現れたら、中止してください。
5)2週間後、皮膚炎の状態を、VASスケールを用いて再評価します。また、写真撮影・血液検査(TARC)も行います。
6)2週間後の再診時に、クロフィブラート軟膏(2分の1の確率で白色ワセリンではなく、確実にクロフィブラート軟膏です)をお渡します。同様に1日1回外用してください。
7)4週間後、3回目の写真撮影・皮疹のVAS評価・血液検査(TARC値)を受けてください。以上で終了です。
8)治験開始前に行っていた治療はそのまま継続してかまいません。
※注 ここで担当医から渡される軟膏は、1)クロフィブラートを含有する軟膏、2)クロフィブラートを含有しないただの白色ワセリン、のどちらかです (確率は2分の1)。担当医にもわかりません。このような手法は、「ブラインドテスト」と言って、そのお薬が本当に効果があるのか?を確認するために必須なことです。「お薬を使った」ということで、皮膚炎が良くなったような気がしてしまう「プラセボ効果」や、たまたま他の理由で皮膚炎がよくなったケースを統計的に排除するためです。
(1)Efficacy of Combined Peroxisome Proliferator-Activated Receptor-α Ligand and Glucocorticoid Therapy in a Murine Model of Atopic Dermatitis Yutaka Hatano Journal of Investigative Dermatology (2011) 131, 1845–1852
(2)Topical application of PPARα (but not β/δ or γ) suppresses atopic dermatitis in NC/Nga mice. Chiba T et al. Allergy. 2012 Jul;67(7):936-42.
<申し込み方法>
同意書(3ページ目)に署名し、住所・電話番号・FAX番号を記入の上、当方までFAX(052-264-0213)してください。年齢・性別のマッチしたペアが出来ましたら、折り返し当方から電話し、受診日時を決めます。
<被験者となるための条件>
今回の被験者は、「ステロイド外用中止後 、軽度のリバウンド( 悪化 )をきたしているが、ステロイドの再使用 を望 まない患者」です。ステロイドを使用中の患者は今回の対象ではありません。
皮疹の程度は、白色ワセリンが外用できる程度の患者です。リバウンドが酷く浸出傾向の強いケースも今回の対象ではありません。
年齢は15 才以上の男女です。幼小児は今回は対象外です。
一回目の診察時に、これまでの臨床経過の問診・皮疹の確認をしますが、その結果、今回の治験には向かないと判断された場合には、お断りする可能性があります。この点御了解ください。
<費用など>
被験者(患者)側の金銭負担はありません。また、本研究は、一開業医である深谷の個人的な関心によるものであり、薬剤費・検査費などは深谷個人の負担です。製薬会社からの資金提供などは一切ありません。
治験責任者 深谷元継(鶴舞公園クリニック院長、日本皮膚科学会認定皮膚科専門医)
460-0012名古屋市中区千代田5-20-6
TEL052-264-0212 FAX052-264-0213
~~~~~~~~~~~~~~~~同 意 書~~~~~~~~~~~~~~~~
私は、上記内容を確認し理解したうえで、今回のクロフィブラート軟膏試用の治験に参加します。
平成 年 月 日 氏名
年齢 才 性別 ( 男・女 )
住所
TEL FAX
(未成年の場合は、同意したことを示す保護者の署名 )
ーーーーー(ここまで)-----
ただし、以前から繰り返し記しているように、わたしは、アトピー性皮膚炎の脱ステロイド診療にたずさわって、自分自身の健康を害した医師です。
こうやって、論文を読んだり、昔の経験を記すことができる程度には回復しましたが、リアルな患者に接することで、ふたたび自分の心身に不調が生じることを、非常に怖れています。
「まだ自分には無理だ」と感じたら、申し訳ありませんが、途中で終了させていただく可能性があります。
今回、できるだけ、淡々と、事務的に診察をすすめたいと考えています。 申し訳ありませんが、効果確認のための診察以上のことは、期待しないでください。
皆様と同じように、わたしもまた、病気から回復しきってはいません。どうかご理解ください。
2012.07.07
3)血液検査をします。TARCというアトピー性皮膚炎の病勢の指標となる検査項目です。
4)担当医から処方された軟膏(※注)を外用します。1日1回、皮膚炎の個所にFTU(フィンガーチップユニット)の考えに準じて外用します。すなわち、大人の人差し指先端から第一関節までの一すくい分を、大人の手のひら二つ分くらいの面積に外用します。これを2週間続けてください。ただし、かぶれなど、肌に合わない兆候が現れたら、中止してください。
5)2週間後、皮膚炎の状態を、VASスケールを用いて再評価します。また、写真撮影・血液検査(TARC)も行います。
6)2週間後の再診時に、クロフィブラート軟膏(2分の1の確率で白色ワセリンではなく、確実にクロフィブラート軟膏です)をお渡します。同様に1日1回外用してください。
7)4週間後、3回目の写真撮影・皮疹のVAS評価・血液検査(TARC値)を受けてください。以上で終了です。
8)治験開始前に行っていた治療はそのまま継続してかまいません。
※注 ここで担当医から渡される軟膏は、1)クロフィブラートを含有する軟膏、2)クロフィブラートを含有しないただの白色ワセリン、のどちらかです (確率は2分の1)。担当医にもわかりません。このような手法は、「ブラインドテスト」と言って、そのお薬が本当に効果があるのか?を確認するために必須なことです。「お薬を使った」ということで、皮膚炎が良くなったような気がしてしまう「プラセボ効果」や、たまたま他の理由で皮膚炎がよくなったケースを統計的に排除するためです。
(1)Efficacy of Combined Peroxisome Proliferator-Activated Receptor-α Ligand and Glucocorticoid Therapy in a Murine Model of Atopic Dermatitis Yutaka Hatano Journal of Investigative Dermatology (2011) 131, 1845–1852
(2)Topical application of PPARα (but not β/δ or γ) suppresses atopic dermatitis in NC/Nga mice. Chiba T et al. Allergy. 2012 Jul;67(7):936-42.
<申し込み方法>
同意書(3ページ目)に署名し、住所・電話番号・FAX番号を記入の上、当方までFAX(052-264-0213)してください。年齢・性別のマッチしたペアが出来ましたら、折り返し当方から電話し、受診日時を決めます。
<被験者となるための条件>
今回の被験者は、「ステロイド外用中止後 、軽度のリバウンド( 悪化 )をきたしているが、ステロイドの再使用 を望 まない患者」です。ステロイドを使用中の患者は今回の対象ではありません。
皮疹の程度は、白色ワセリンが外用できる程度の患者です。リバウンドが酷く浸出傾向の強いケースも今回の対象ではありません。
年齢は15 才以上の男女です。幼小児は今回は対象外です。
一回目の診察時に、これまでの臨床経過の問診・皮疹の確認をしますが、その結果、今回の治験には向かないと判断された場合には、お断りする可能性があります。この点御了解ください。
<費用など>
被験者(患者)側の金銭負担はありません。また、本研究は、一開業医である深谷の個人的な関心によるものであり、薬剤費・検査費などは深谷個人の負担です。製薬会社からの資金提供などは一切ありません。
治験責任者 深谷元継(鶴舞公園クリニック院長、日本皮膚科学会認定皮膚科専門医)
460-0012名古屋市中区千代田5-20-6
TEL052-264-0212 FAX052-264-0213
~~~~~~~~~~~~~~~~同 意 書~~~~~~~~~~~~~~~~
私は、上記内容を確認し理解したうえで、今回のクロフィブラート軟膏試用の治験に参加します。
平成 年 月 日 氏名
年齢 才 性別 ( 男・女 )
住所
TEL FAX
(未成年の場合は、同意したことを示す保護者の署名 )
ーーーーー(ここまで)-----
ただし、以前から繰り返し記しているように、わたしは、アトピー性皮膚炎の脱ステロイド診療にたずさわって、自分自身の健康を害した医師です。
こうやって、論文を読んだり、昔の経験を記すことができる程度には回復しましたが、リアルな患者に接することで、ふたたび自分の心身に不調が生じることを、非常に怖れています。
「まだ自分には無理だ」と感じたら、申し訳ありませんが、途中で終了させていただく可能性があります。
今回、できるだけ、淡々と、事務的に診察をすすめたいと考えています。 申し訳ありませんが、効果確認のための診察以上のことは、期待しないでください。
皆様と同じように、わたしもまた、病気から回復しきってはいません。どうかご理解ください。
2012.07.07