佐賀大学のペリオスチン経路とPPARリガンドとの関係
佐賀大学分子医科学教室が解明したペリオスチンを介するアトピー性皮膚炎の難治化メカニズムは非常に重要だと思います。ステロイド依存という現象が説明できるからです(→こちら)。
ところで、少し前ですが、ステロイド外用時にPPAR結合物質を併用すると、離脱時のリバウンドが起きにくいようだ、という論文について解説しました(→こちらとこちら)。
ペリオスチン経路と、PPARリガンドの作用点とは、関係があるのでしょうか?そう思いついて、Pubmed(医学論文データベース)で、「periostin」と「PPAR」のキーワードで検索してみました。それで見つけたのが、今回紹介する論文です。
Peroxisome proliferator-activated receptor γ-mediated suppression of dendritic cell function prevents the onset of atopic dermatitis in NC/Tnd mice.Jung K et al. J Allergy Clin Immunol. 2011 Feb;127(2):420-429
東京農大の獣医分子病態治療学研究室(→こちら)発の論文です。佐賀大学の研究も基礎医学教室発のもので、いづれも皮膚科学教室発でない点は寂しいところですが・・。 PPAR結合物質としては、PPARγアゴニスト(リガンド)のロシグリタゾン(rosiglitazone)という薬剤を用いています。日本では未発売ですが、2型糖尿病の内服薬として製品化されているものです。
ところで、少し前ですが、ステロイド外用時にPPAR結合物質を併用すると、離脱時のリバウンドが起きにくいようだ、という論文について解説しました(→こちらとこちら)。
ペリオスチン経路と、PPARリガンドの作用点とは、関係があるのでしょうか?そう思いついて、Pubmed(医学論文データベース)で、「periostin」と「PPAR」のキーワードで検索してみました。それで見つけたのが、今回紹介する論文です。
Peroxisome proliferator-activated receptor γ-mediated suppression of dendritic cell function prevents the onset of atopic dermatitis in NC/Tnd mice.Jung K et al. J Allergy Clin Immunol. 2011 Feb;127(2):420-429
東京農大の獣医分子病態治療学研究室(→こちら)発の論文です。佐賀大学の研究も基礎医学教室発のもので、いづれも皮膚科学教室発でない点は寂しいところですが・・。 PPAR結合物質としては、PPARγアゴニスト(リガンド)のロシグリタゾン(rosiglitazone)という薬剤を用いています。日本では未発売ですが、2型糖尿病の内服薬として製品化されているものです。
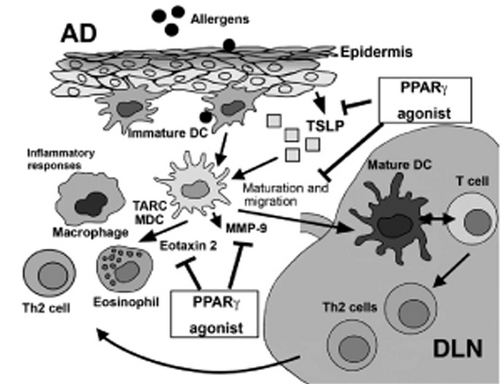
論文の末尾にイラストがあります。
PPARγアゴニストは、表皮細胞から産生されるTSLPに拮抗して、ランゲルハンス細胞(樹枝状細胞:DC)の成熟や所属リンパ節(DLN)への遊走を妨げます。また、TARCやMMP-9といった物質の産生をも妨げます。そういった内容です。
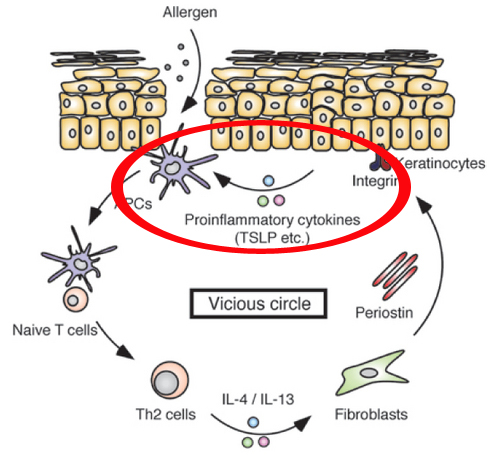
このTSLPのランゲルハンス細胞への作用というのは、佐賀大学の論文のイラストでいうと、赤丸で囲んだ部分です。
このTSLPのランゲルハンス細胞への作用というのは、佐賀大学の論文のイラストでいうと、赤丸で囲んだ部分です。
ですから、PPARγアゴニストを用いれば、佐賀大学が今後、研究開発を目指している、ペリオスチンに対する抗体を用いて、このペリオスチン経路(悪循環=vicious circle)を断ち切ろうとしているのと、同じ効果が得られる可能性があります。
実際、「ステロイド外用時にPPAR結合物質を併用すると、離脱時のリバウンドが起きにくいようだ」とする大分大学の波多野先生の論文(→こちら)は、それを示唆しています。
PPARアゴニストとしては、PPARαリガンドであるクロフィブラートが、表皮細胞のフィラグリン・インボルクリンなどの蛋白質の産生を促して、ステロイドによる表皮バリア破壊の抑制効果がある、という点から、これを軟膏として用いることで、ステロイド依存の予防になるのではないか?(→こちら)と提案しました。クロフィブラートは安価で入手しやすいからです。
ロシグリタゾンは日本未発売のため入手はやや難ですが、医師の個人輸入で手に入れようと思えば出来ます(わたしは美容外科医なので、その手のことには慣れています)。
問題点は、ひとつあって、ロシグリタゾンは、糖尿病の薬として広く使われていたのですが、心不全の合併症が問題視されて、現在販売縮小傾向です。もしも軟膏に練って使う場合には、内服並みに血中濃度が上がることのないようにしなければなりません。大量の外用には向いていないでしょう。
クロフィブラートについては、そのような警告はなく、日本でも普通に販売されている内服薬なので、注意は少なくて済むはずです。クロフィブラート(PPARαリガンド)とロシグリタゾン(PPARγリガンド)は、まったく同じではありませんが、フィラグリン発現などの効果を見ても、作用は似ています。ですから、東京農大の論文と似た効果が、クロフィブラートを用いても得られる可能性が高いと思います。
昔の仲間の脱ステ医たちと相談して、クロフィブラートまたはロシグリタゾン軟膏を活用できないか、検討してみようかと思います。
PPARリガンドの軟膏は、単独では炎症を抑えるまでの力は無いようですし(→こちら)、「ステロイド依存の予防となる」あるいは「リバウンドを沈静化させる」という効能は、ステロイド依存の存在そのものを認めようとしない現在の皮膚科学会の風潮からは、当分検討されないと思われるので。
具体的な方法ですが、わたしがクロフィブラートまたはロシグリタゾン軟膏を作製して、協力医師を介して、患者に使用してもらい、患者側評価・医師側評価・血液検査(メカニズムから考えてTARCが適当と思われる)・副作用について検討すればよいと思われます。
軟膏基剤(白色ワセリンまたは亜鉛華単軟膏)とを、年齢・性をマッチさせて、患者・協力医師にはブラインドで配布すれば、RCTが可能です。
対象患者は、1)ステロイド使用中、2)離脱直後、3)離脱後長期経過後、に分けるといいと思います。評価期間は、とりあえず二週間くらいかなあ?・・TARCを健康保険で検査してもらうなら、査定の関係から、1ヶ月開けたほうがいいかもしれませんが。
クロフィブラートまたはロシグリタゾン軟膏作製および郵送費用については、当方としては、一切費用は要りません。軟膏基剤にしろ、クロフィブラート・ロシグリタゾンにしろ、大した額ではないからです。軟膏調整については、当方シンキーの「あわとり練太郎」を持っているので大丈夫です。患者負担は、TARC検査費用だけで済みます。
協力いただける皮膚科医のかたいらっしゃいましたら、コメント欄を通じてご連絡ください。とくに、ステロイド使用中の患者でのデータは、私の知人の脱ステ医のところでは、集まりにくいと思われるので、ご協力いただけると助かります。研究計画についても、だいたい上記のようなイメージですが、変更は可能です。
補足)
Topical application of PPARα (but not β/δ or γ) suppresses atopic dermatitis in NC/Nga mice.
Chiba T et al. Allergy. 2012 Jul;67(7):936-42.
上記論文によると、マウスのデータではありますが、実際に外用して皮膚炎やTarc値、IgEを抑える効果があったのは、PPARのうちのαのみで、β/δ やγでは効果が認められなかったようです。
実際、「ステロイド外用時にPPAR結合物質を併用すると、離脱時のリバウンドが起きにくいようだ」とする大分大学の波多野先生の論文(→こちら)は、それを示唆しています。
PPARアゴニストとしては、PPARαリガンドであるクロフィブラートが、表皮細胞のフィラグリン・インボルクリンなどの蛋白質の産生を促して、ステロイドによる表皮バリア破壊の抑制効果がある、という点から、これを軟膏として用いることで、ステロイド依存の予防になるのではないか?(→こちら)と提案しました。クロフィブラートは安価で入手しやすいからです。
ロシグリタゾンは日本未発売のため入手はやや難ですが、医師の個人輸入で手に入れようと思えば出来ます(わたしは美容外科医なので、その手のことには慣れています)。
問題点は、ひとつあって、ロシグリタゾンは、糖尿病の薬として広く使われていたのですが、心不全の合併症が問題視されて、現在販売縮小傾向です。もしも軟膏に練って使う場合には、内服並みに血中濃度が上がることのないようにしなければなりません。大量の外用には向いていないでしょう。
クロフィブラートについては、そのような警告はなく、日本でも普通に販売されている内服薬なので、注意は少なくて済むはずです。クロフィブラート(PPARαリガンド)とロシグリタゾン(PPARγリガンド)は、まったく同じではありませんが、フィラグリン発現などの効果を見ても、作用は似ています。ですから、東京農大の論文と似た効果が、クロフィブラートを用いても得られる可能性が高いと思います。
昔の仲間の脱ステ医たちと相談して、クロフィブラートまたはロシグリタゾン軟膏を活用できないか、検討してみようかと思います。
PPARリガンドの軟膏は、単独では炎症を抑えるまでの力は無いようですし(→こちら)、「ステロイド依存の予防となる」あるいは「リバウンドを沈静化させる」という効能は、ステロイド依存の存在そのものを認めようとしない現在の皮膚科学会の風潮からは、当分検討されないと思われるので。
具体的な方法ですが、わたしがクロフィブラートまたはロシグリタゾン軟膏を作製して、協力医師を介して、患者に使用してもらい、患者側評価・医師側評価・血液検査(メカニズムから考えてTARCが適当と思われる)・副作用について検討すればよいと思われます。
軟膏基剤(白色ワセリンまたは亜鉛華単軟膏)とを、年齢・性をマッチさせて、患者・協力医師にはブラインドで配布すれば、RCTが可能です。
対象患者は、1)ステロイド使用中、2)離脱直後、3)離脱後長期経過後、に分けるといいと思います。評価期間は、とりあえず二週間くらいかなあ?・・TARCを健康保険で検査してもらうなら、査定の関係から、1ヶ月開けたほうがいいかもしれませんが。
クロフィブラートまたはロシグリタゾン軟膏作製および郵送費用については、当方としては、一切費用は要りません。軟膏基剤にしろ、クロフィブラート・ロシグリタゾンにしろ、大した額ではないからです。軟膏調整については、当方シンキーの「あわとり練太郎」を持っているので大丈夫です。患者負担は、TARC検査費用だけで済みます。
協力いただける皮膚科医のかたいらっしゃいましたら、コメント欄を通じてご連絡ください。とくに、ステロイド使用中の患者でのデータは、私の知人の脱ステ医のところでは、集まりにくいと思われるので、ご協力いただけると助かります。研究計画についても、だいたい上記のようなイメージですが、変更は可能です。
補足)
Topical application of PPARα (but not β/δ or γ) suppresses atopic dermatitis in NC/Nga mice.
Chiba T et al. Allergy. 2012 Jul;67(7):936-42.
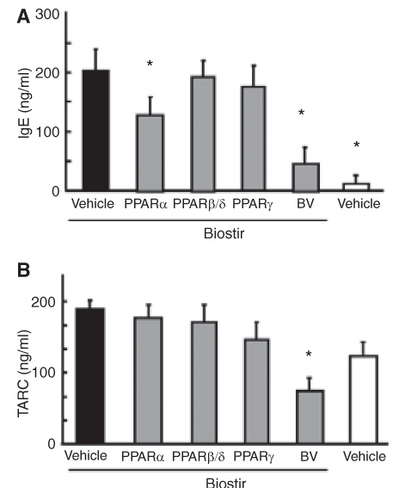
上記論文によると、マウスのデータではありますが、実際に外用して皮膚炎やTarc値、IgEを抑える効果があったのは、PPARのうちのαのみで、β/δ やγでは効果が認められなかったようです。
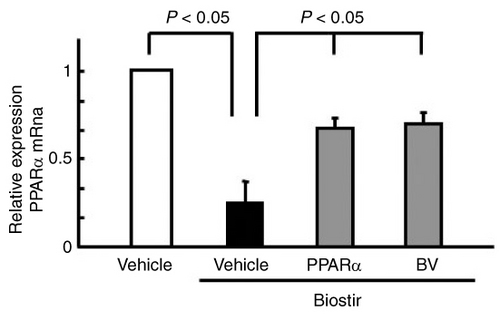
(BVはステロイド、Biostirはダニ抗原です)
また、上記論文では、ステロイドの外用は、表皮細胞のPPARα発現を増加させることも示しています。
また、上記論文では、ステロイドの外用は、表皮細胞のPPARα発現を増加させることも示しています。
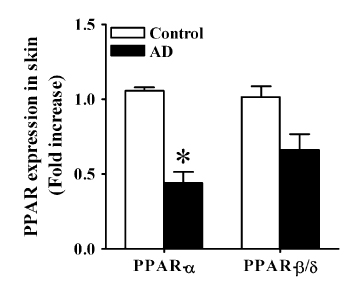
一方、下記論文によると、
Peroxisome proliferator-activated receptor alpha regulates skin inflammation and humoral response in atopic dermatitis.
Staumont-Sallé D et al. J Allergy Clin Immunol. 2008 Apr;121(4):962-8.
アトピー性皮膚炎患者では、表皮細胞のPPARα発現が低下しているようです。
Peroxisome proliferator-activated receptor alpha regulates skin inflammation and humoral response in atopic dermatitis.
Staumont-Sallé D et al. J Allergy Clin Immunol. 2008 Apr;121(4):962-8.
アトピー性皮膚炎患者では、表皮細胞のPPARα発現が低下しているようです。
これらをどう解釈するかというと、
1)アトピー性皮膚炎患者ではPPARαが低下している。
2)PPARαは、おそらくγと同じようにTSLP→DC(ランゲルハンス細胞)を抑えることによって、抗炎症作用がある(東京農大の論文はγに関するものだが、αでデータを取っても、同等以上の結果が得られただろう)。
3)ステロイド外用はPPARαを増やす。
4)ステロイド外用は、また、表皮からDC(ランゲルハンス細胞)を減少させる(→こちら)。ステロイド外用中は、TSLP→DCの悪化サイクルがⅰ)DC減少とⅱ)PPARα増加でブロックされていると考えられる。
5)ステロイド外用によってPPARαが増加するのなら、PPARαの外用はステロイド外用中には効果が少ない。離脱後のリバウンド時、またはステロイドを使用していない患者においてこそ効果が期待できそうだ。
というように、私は考えます。
2012.06
1)アトピー性皮膚炎患者ではPPARαが低下している。
2)PPARαは、おそらくγと同じようにTSLP→DC(ランゲルハンス細胞)を抑えることによって、抗炎症作用がある(東京農大の論文はγに関するものだが、αでデータを取っても、同等以上の結果が得られただろう)。
3)ステロイド外用はPPARαを増やす。
4)ステロイド外用は、また、表皮からDC(ランゲルハンス細胞)を減少させる(→こちら)。ステロイド外用中は、TSLP→DCの悪化サイクルがⅰ)DC減少とⅱ)PPARα増加でブロックされていると考えられる。
5)ステロイド外用によってPPARαが増加するのなら、PPARαの外用はステロイド外用中には効果が少ない。離脱後のリバウンド時、またはステロイドを使用していない患者においてこそ効果が期待できそうだ。
というように、私は考えます。
2012.06