安保徹先生の「酸化コレステロール仮説」について
新潟大学医学部の、皮膚科ではなく医動物学教室という基礎講座の前教授で、一般向けの図書なども多く著していらっしゃる安保徹先生という方がいらっしゃいます。彼は「ステロイド皮膚症(リバウンド)の原因は、外用したステロイドが局所で酸化されて生じた酸化コレステロールが炎症を惹起するからである」という仮説を提唱していました。
私は1999年に「ステロイド依存―ステロイドをやめたいアトピー性皮膚炎患者のために」という本を著したのですが、安保先生はこれを非常に好意的にご自身の著作の中で取り上げて紹介してくださいました(たとえば→治療、82, 6, 1794-1803, 2000)。
私はというと、安保先生のこの仮説には非常に戸惑いを感じました。というのは、仮説のよりどころとなる基礎論文がまったく無かったからです。ステロイドを外用した皮膚は、外用していない皮膚に比べて酸化コレステロールが多く沈着しているといった、動物実験でも患者の皮膚でもいいのですが、根拠のような論文があるのだろうか?と、当時調べてみたのですが、どうもそういうものはなく、安保先生が、まったく直観的に構築した仮説であるように思われました。
外用したステロイドがどのように吸収されていくかについては、オートラジオグラフィーなどを用いて追跡した論文が古くからあります。例えば、
コルチコステロイドの皮膚吸収および皮膚貯留現象に関する研究 松沢徹 日皮会誌 80(7) 428-446, 1970
(下記リンクで全文が公開されています )
http://drmtl.org/data/080070428.pdf
これを読むと、外用ステロイドというのは、種類にもよりますが、一回の外用(24時間ODT)後数日以内に皮膚から消失しています(毛嚢や脂腺には7日後も若干残ります)。
この事実一つをとっても、安保先生の仮説は受け入れ難いです。
しかし、その一方で、安保先生の仮説は、最近の医学論文に照らし合わせると、ステロイド依存のメカニズムを考える上で、ひょっとしたら大きなヒントを与えてくれていたのかもしれない、とも感じます。今回はその点について記します。
まず第一に、あまり認識されていない事実だと思いますが、血液中と組織中とでは、生理的なコルチゾールの濃度が異なります。
例えば、熱傷患者の血漿および組織中のコルチゾール濃度を調べた下の論文では、血漿中総コルチゾールは8.8μg/dlで遊離コルチゾールが1.7μg/dlに対し、組織中コルチゾールは0.74μg/dlでした。
Measurement of tissue cortisol levels in patients with severe burns: a preliminary investigation.Cohen J et al, Crit Care. 2009;13(6):R189. Epub 2009 Nov 27.
対照として測定された健常者の組織中コルチゾールは0.20μg/dlです(熱傷患者の組織コルチゾール値は亢進しているということ)。ですから、組織中コルチゾール値は、血漿コルチゾール値の数十分の一、血漿遊離コルチゾールの数分の一と考えていいです。血中にストックされているコルチゾールは担体と結合していて、必要に応じて、組織に供給されるという仕組みです。
なぜこういうことになっているかというと、血管外組織においては、本来ステロイドは高濃度で存在すべきではない、熱傷など炎症が生じた時点で、これに関与すべく動員される、ということなのでしょう。
とすると、ステロイドを外用するということは、実はとんでもない負荷を、血管外組織である皮膚に対してかけているということなのかもしれません。内服のステロイドは、吸収されて血中に留まりますから、皮膚組織での濃度上昇は、血管壁の制御下にあります。
第二に、表皮細胞(および毛嚢の細胞も)や、真皮の繊維芽細胞は、それ自身がステロイドを産生している、という事実が判ってきました。また、これを活性型と非活性型、相互に変換する酵素(11βHSD1および2)を持っています。
私は1999年に「ステロイド依存―ステロイドをやめたいアトピー性皮膚炎患者のために」という本を著したのですが、安保先生はこれを非常に好意的にご自身の著作の中で取り上げて紹介してくださいました(たとえば→治療、82, 6, 1794-1803, 2000)。
私はというと、安保先生のこの仮説には非常に戸惑いを感じました。というのは、仮説のよりどころとなる基礎論文がまったく無かったからです。ステロイドを外用した皮膚は、外用していない皮膚に比べて酸化コレステロールが多く沈着しているといった、動物実験でも患者の皮膚でもいいのですが、根拠のような論文があるのだろうか?と、当時調べてみたのですが、どうもそういうものはなく、安保先生が、まったく直観的に構築した仮説であるように思われました。
外用したステロイドがどのように吸収されていくかについては、オートラジオグラフィーなどを用いて追跡した論文が古くからあります。例えば、
コルチコステロイドの皮膚吸収および皮膚貯留現象に関する研究 松沢徹 日皮会誌 80(7) 428-446, 1970
(下記リンクで全文が公開されています )
http://drmtl.org/data/080070428.pdf
これを読むと、外用ステロイドというのは、種類にもよりますが、一回の外用(24時間ODT)後数日以内に皮膚から消失しています(毛嚢や脂腺には7日後も若干残ります)。
この事実一つをとっても、安保先生の仮説は受け入れ難いです。
しかし、その一方で、安保先生の仮説は、最近の医学論文に照らし合わせると、ステロイド依存のメカニズムを考える上で、ひょっとしたら大きなヒントを与えてくれていたのかもしれない、とも感じます。今回はその点について記します。
まず第一に、あまり認識されていない事実だと思いますが、血液中と組織中とでは、生理的なコルチゾールの濃度が異なります。
例えば、熱傷患者の血漿および組織中のコルチゾール濃度を調べた下の論文では、血漿中総コルチゾールは8.8μg/dlで遊離コルチゾールが1.7μg/dlに対し、組織中コルチゾールは0.74μg/dlでした。
Measurement of tissue cortisol levels in patients with severe burns: a preliminary investigation.Cohen J et al, Crit Care. 2009;13(6):R189. Epub 2009 Nov 27.
対照として測定された健常者の組織中コルチゾールは0.20μg/dlです(熱傷患者の組織コルチゾール値は亢進しているということ)。ですから、組織中コルチゾール値は、血漿コルチゾール値の数十分の一、血漿遊離コルチゾールの数分の一と考えていいです。血中にストックされているコルチゾールは担体と結合していて、必要に応じて、組織に供給されるという仕組みです。
なぜこういうことになっているかというと、血管外組織においては、本来ステロイドは高濃度で存在すべきではない、熱傷など炎症が生じた時点で、これに関与すべく動員される、ということなのでしょう。
とすると、ステロイドを外用するということは、実はとんでもない負荷を、血管外組織である皮膚に対してかけているということなのかもしれません。内服のステロイドは、吸収されて血中に留まりますから、皮膚組織での濃度上昇は、血管壁の制御下にあります。
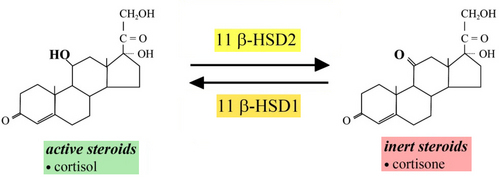
第二に、表皮細胞(および毛嚢の細胞も)や、真皮の繊維芽細胞は、それ自身がステロイドを産生している、という事実が判ってきました。また、これを活性型と非活性型、相互に変換する酵素(11βHSD1および2)を持っています。
表皮細胞や真皮繊維芽細胞は、自分自身の分裂増殖や、リンパ球などの炎症細胞への作用を、自らステロイドを産生することによって調整しています。培養細胞を用いた実験結果によれば、表皮細胞のこの微量なステロイド分泌作用は、ACTHの支配までも受けていることが判っています。
この不活性型のステロイド(コルチゾン=コルチゾールの酸化物)を、安保先生のいう「酸化コレステロール」と置き換えて、安保先生の仮説を翻訳すると、筋が通ってきます。そのような視点で、私が今回の記事を書いているということを念頭に、読み進めてください。
詳細な研究によれば、表皮細胞や真皮繊維芽細胞では11βHSD1が、エックリン汗腺細胞では11βHSD2が、活性が高いことも判明しています。
強力ネオミノファーゲンCの記事のところで、強力ネオミノファーゲンCは11βHSD2を阻害することで、活性型のコルチゾール濃度を高め、抗炎症作用を示す、ということを記しましたが、上記を照らし合わせると、強力ネオミノファーゲンCは汗腺でのコルチゾール の不活化を抑える、ということになりそうです。
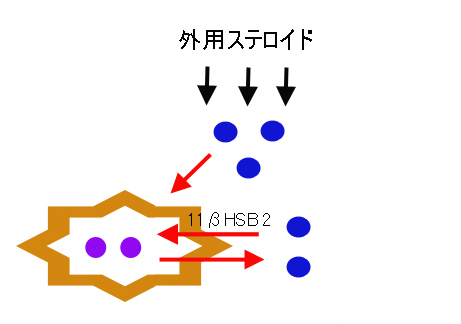
以上をまとめて図にすると、下のようになります。
この不活性型のステロイド(コルチゾン=コルチゾールの酸化物)を、安保先生のいう「酸化コレステロール」と置き換えて、安保先生の仮説を翻訳すると、筋が通ってきます。そのような視点で、私が今回の記事を書いているということを念頭に、読み進めてください。
詳細な研究によれば、表皮細胞や真皮繊維芽細胞では11βHSD1が、エックリン汗腺細胞では11βHSD2が、活性が高いことも判明しています。
強力ネオミノファーゲンCの記事のところで、強力ネオミノファーゲンCは11βHSD2を阻害することで、活性型のコルチゾール濃度を高め、抗炎症作用を示す、ということを記しましたが、上記を照らし合わせると、強力ネオミノファーゲンCは汗腺でのコルチゾール の不活化を抑える、ということになりそうです。
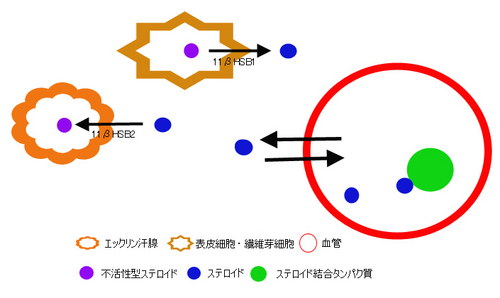
以上をまとめて図にすると、下のようになります。
組織(皮膚)のステロイド濃度は、3つの経路によって制御されています。
1血管内からの移動
2表皮細胞・繊維芽細胞からの産生
3汗腺での不活化(および排泄) です。
さらに興味深いことには、表皮細胞・繊維芽細胞からのコルチゾールの産生には、ステロイド自体による正のフィードバックのメカニズムが存在します。
Localization, age- and site-dependent expression, and regulation of 11β-hydroxysteroid dehydrogenase type 1 in skin.Tiganescu A,J et al. Invest Dermatol. 2011 Jan;131(1):30-6
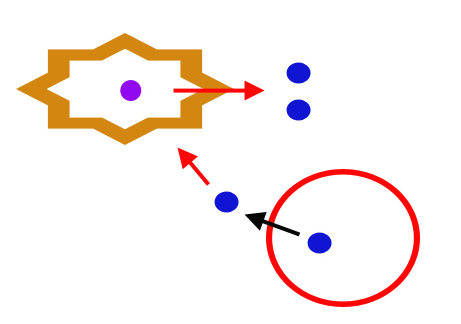
下図のようなイメージです。
1血管内からの移動
2表皮細胞・繊維芽細胞からの産生
3汗腺での不活化(および排泄) です。
さらに興味深いことには、表皮細胞・繊維芽細胞からのコルチゾールの産生には、ステロイド自体による正のフィードバックのメカニズムが存在します。
Localization, age- and site-dependent expression, and regulation of 11β-hydroxysteroid dehydrogenase type 1 in skin.Tiganescu A,J et al. Invest Dermatol. 2011 Jan;131(1):30-6
下図のようなイメージです。
たとえば、血管内から組織にコルチゾールが遊離してくると、これを受けて表皮細胞・繊維芽細胞がさらにコルチゾールを産生するということです。組織の炎症などのストレスに対して、迅速にコルチゾール濃度を上げる仕組みです。
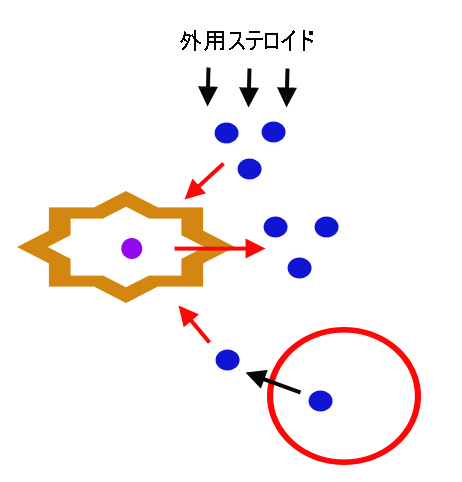
さて、このような、絶妙なコントロール下にある組織(皮膚)に、外用と言う形で、直接ステロイドが投与されるとどうなるでしょうか?
表皮細胞・真皮繊維芽細胞は、ステロイドによる正のフィードバックを受けますから、外用ステロイドにも反応して、目いっぱいコルチゾールの産生を始めるでしょう。
さて、このような、絶妙なコントロール下にある組織(皮膚)に、外用と言う形で、直接ステロイドが投与されるとどうなるでしょうか?
表皮細胞・真皮繊維芽細胞は、ステロイドによる正のフィードバックを受けますから、外用ステロイドにも反応して、目いっぱいコルチゾールの産生を始めるでしょう。
外用ステロイドは表皮細胞・真皮繊維芽細胞の分裂増殖を休止させて皮膚を萎縮させますが、このメカニズムには、実は、表皮細胞・真皮繊維芽細胞自身も一役買ってるということになります。
ステロイド外用をやめるとどうなるのでしょうか?
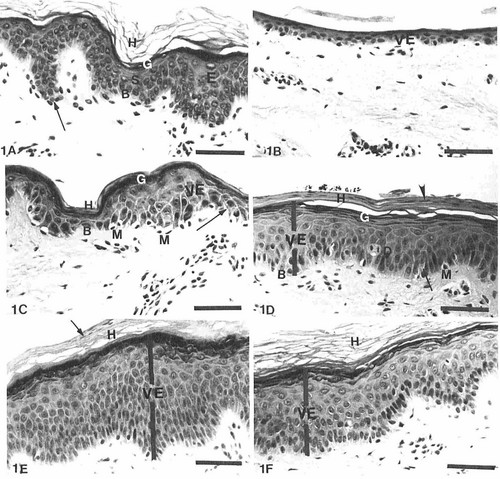
以前紹介した、健常皮膚に強力なステロイドを外用したのち中止したあとの皮膚の組織学的変化の写真を振り返ってみましょう。
ステロイド外用をやめるとどうなるのでしょうか?
以前紹介した、健常皮膚に強力なステロイドを外用したのち中止したあとの皮膚の組織学的変化の写真を振り返ってみましょう。
(Morphologic Investigations on the Rebound Phenomenon After Corticosteroid Induced Atrophy in Human Skin. Zheng P, et al. J Invest Dermatol 82: 345-352, 1984)
1Aは外用開始前で、1Bが外用して萎縮した表皮です。中止後、1C,1D,1Eのように、表皮は反動で前よりも一時的に厚みを増しています。これは、外用ステロイド中止後、一時的に皮膚がステロイド不足に陥り、その結果表皮細胞の分裂増殖が亢進した結果と考えられます。
なぜ、中止後にステロイド不足に陥るのか?ここが説明できません。以下はあくまで私の考えですが、
1、外用ステロイド長期連用後は、11βHSD2が一時的に優位になるのではないか? ステロイド外用が長期にわたると、あまりに過剰に存在する組織のステロイド濃度を減ずるために、表皮自身が通常とは逆のコルチゾール不活化の経路を活用し始めるのではないか。
1Aは外用開始前で、1Bが外用して萎縮した表皮です。中止後、1C,1D,1Eのように、表皮は反動で前よりも一時的に厚みを増しています。これは、外用ステロイド中止後、一時的に皮膚がステロイド不足に陥り、その結果表皮細胞の分裂増殖が亢進した結果と考えられます。
なぜ、中止後にステロイド不足に陥るのか?ここが説明できません。以下はあくまで私の考えですが、
1、外用ステロイド長期連用後は、11βHSD2が一時的に優位になるのではないか? ステロイド外用が長期にわたると、あまりに過剰に存在する組織のステロイド濃度を減ずるために、表皮自身が通常とは逆のコルチゾール不活化の経路を活用し始めるのではないか。
もしそうだとすれば、これは安保先生の仮説の「酸化コレステロールの蓄積」のイメージに似ています。
外用ステロイドそのものの酸化物ではなく、外用ステロイドの影響によって内因性のステロイド(コルチゾール)が不活性型の酸化物であるコルチゾンとなって、細胞のどこかに蓄積されているのではないか?ということです。もともと、組織での需要に応じて、すばやくコルチゾン→コルチゾールに変換して分泌するメカニズムですから、コルチゾンの貯留場所は存在するはずです。
ステロイド外用中止後、一過性に表皮が肥大する理由としては、このほかに、
2、汗腺での11βHSD2が亢進する。
3、ステロイドレセプターが減少していている(ステロイドに対する感度が鈍くなっている)。
といったことも考えられます。いずれにせよ、上図のように、ステロイド中止後一過性に表皮が厚さを増すということは、組織(皮膚)中でステロイドが、相対的な不足となることを意味しています。そのメカニズムとして、私は上記の3つしか思いつきません。
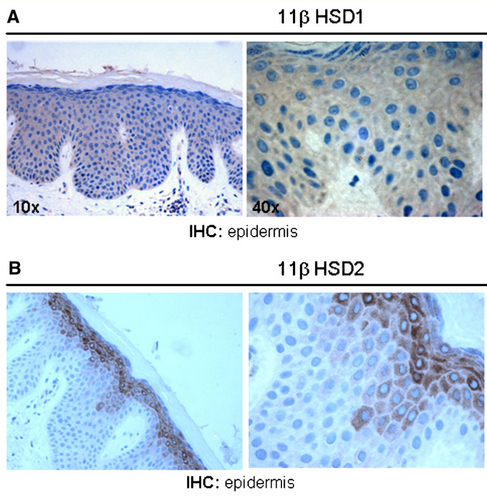
下図は、健常皮膚における、表皮における11βHSD1/2の分布です。11βHSD1は基底層からマルピギー層にかけて存在しますが、11βHSD2は顆粒細胞層から角層にかけて局在しています(茶色に染まっているのが11βHSD1/2です)。
(注)私が実際に染色してみた結果では、HSD2はたしかに上層で染まる症例もあるのですが、どうも基底層で染まる症例のほうが多いようです(→こちら)。また、ステロイド外用後はHSD-2は表皮全体が染色されるようです(→こちら)。
外用ステロイドそのものの酸化物ではなく、外用ステロイドの影響によって内因性のステロイド(コルチゾール)が不活性型の酸化物であるコルチゾンとなって、細胞のどこかに蓄積されているのではないか?ということです。もともと、組織での需要に応じて、すばやくコルチゾン→コルチゾールに変換して分泌するメカニズムですから、コルチゾンの貯留場所は存在するはずです。
ステロイド外用中止後、一過性に表皮が肥大する理由としては、このほかに、
2、汗腺での11βHSD2が亢進する。
3、ステロイドレセプターが減少していている(ステロイドに対する感度が鈍くなっている)。
といったことも考えられます。いずれにせよ、上図のように、ステロイド中止後一過性に表皮が厚さを増すということは、組織(皮膚)中でステロイドが、相対的な不足となることを意味しています。そのメカニズムとして、私は上記の3つしか思いつきません。
下図は、健常皮膚における、表皮における11βHSD1/2の分布です。11βHSD1は基底層からマルピギー層にかけて存在しますが、11βHSD2は顆粒細胞層から角層にかけて局在しています(茶色に染まっているのが11βHSD1/2です)。
(注)私が実際に染色してみた結果では、HSD2はたしかに上層で染まる症例もあるのですが、どうも基底層で染まる症例のほうが多いようです(→こちら)。また、ステロイド外用後はHSD-2は表皮全体が染色されるようです(→こちら)。
(Keratinocytes synthesize and activate cortisol.Cirillo et al.J Cell Biochem. 2011 Jun;112(6):1499-505)
長期にステロイド外用を続けて中止したあとでは、この11βHSD1/2のバランスが乱れているはずです。表皮細胞、あるいは真皮基底細胞、汗腺細胞の、11βHSD1/2のバランスの乱れが、リバウンドや、離脱後の過敏性の続く皮膚の真の原因なのかもしれません。
ステロイド長期外用後の副作用である表皮バリア破壊は、この11βHSD1/2のバランスの乱れによる二次的な現象かもしれません。
ステロイド長期外用中および、中止後の患者の皮膚を、11βHSD1/2で、上図と同じように免疫染色してパターン分類してやると、いろいろ興味深い所見が得られると思います・・どなたか、大学などで研究現場にいらっしゃる方、やってみませんか?(^^;。
抗体購入費用など、若干の研究費は、もしよろしければ私が提供します。もしも、11βHSD1/2の染色パターンで、ステロイド長期外用からの回復状況が解るなら、ステロイド依存や離脱の臨床にとって、大きなツールとなり得るからです。
2013.07.08
長期にステロイド外用を続けて中止したあとでは、この11βHSD1/2のバランスが乱れているはずです。表皮細胞、あるいは真皮基底細胞、汗腺細胞の、11βHSD1/2のバランスの乱れが、リバウンドや、離脱後の過敏性の続く皮膚の真の原因なのかもしれません。
ステロイド長期外用後の副作用である表皮バリア破壊は、この11βHSD1/2のバランスの乱れによる二次的な現象かもしれません。
ステロイド長期外用中および、中止後の患者の皮膚を、11βHSD1/2で、上図と同じように免疫染色してパターン分類してやると、いろいろ興味深い所見が得られると思います・・どなたか、大学などで研究現場にいらっしゃる方、やってみませんか?(^^;。
抗体購入費用など、若干の研究費は、もしよろしければ私が提供します。もしも、11βHSD1/2の染色パターンで、ステロイド長期外用からの回復状況が解るなら、ステロイド依存や離脱の臨床にとって、大きなツールとなり得るからです。
2013.07.08
私が作製した中間分子量ヒアルロン酸化粧水「ヒアルプロテクト」のショップはこちら(下の画像をクリック)