アトピー性皮膚炎患者へのステロイド外用は表皮におけるコルチゾールの恒常性に影響を与える
Indian Journal of Dermatologyに投稿していたアトピー性皮膚炎の免疫組織学的研究の論文が上梓されました(→こちら)。こちらに日本語の翻訳を掲示しておきます。
先回の6か月調査の論文(→こちら)は、疫学的なものですが、今回は基礎的な面からの研究です。こうして手を替え品を替えてPubmed収載の医学論文として報告していけば、いつかタブーが崩れて、皮膚科医たちが真剣にこの問題を議論する日が来るでしょう。そう信じます。
☆ーーーーー☆ーーーーー☆ーーーーー☆ーーーーー☆
アトピー性皮膚炎患者へのステロイド外用は表皮におけるコルチゾールの恒常性に影響を与える
要約
背景:
皮膚はコルチゾールを産生し自身の増殖・分化を調節している。ステロイド外用剤は皮膚におけるコルチゾールの恒常性に影響を与える可能性がある。
目的と対象:
ステロイド外用後の表皮におけるコルチゾールおよびその関連物質の分布と濃度の免疫組織学的検討。
材料と方法:
1人の健常人男性の前腕にclobetasol propionate 0.05%(デルモベート軟膏)を二週間一日二回外用し、前後で皮膚を生検した。採取した皮膚をMLN64, StAR, CPY11A1, cortisol, HSD11B1, HSD11B2, GRA, GRB, MCR に対する各種抗体で免疫染色した。同様の皮膚生検を19人の長期間ステロイド外用の経験のある成人アトピー性皮膚炎患者において行った。患者の内訳は、現在ステロイド外用剤使用中(TCS +)が4名、現在ステロイド外用剤を使用しておらず生検部(前腕)に皮疹のある患者(TCS-E+)が12名、ステロイド外用剤を使用しておらず生検部に皮疹がない患者(TCS-E-)が3名である。
結果:
健常人ボランティアにおけるMLN64, cortisol, HSD11B2の染色強度はステロイド外用中増加した。TCS-E+ 患者においては、TCS + 患者や TCS-E-患者よりも基底層でHSD11B2が、有棘層でMCR の染色が強かった。またTCS-E+ 患者においては、TCS + 患者や TCS-E-患者よりも基底層と顆粒層でのMLN64染色が弱く、基底層でのHSD11B1 の染色が弱く、全層のGRB の染色が弱かった。
結論:
TCS-E+患者にみられる表皮の肥厚と不全角化は、MLN64によって調節されるコルチゾール合成能の低下と、HSD11B2によるコルチゾールの不活性化によるのかもしれない。GRB の減少とMCR の増加は角化細胞におけるコルチゾールの反応性を高めているのかもしれない。
はじめに
ステロイド外用剤は有用で一般的な皮膚科領域の薬剤であり、さまざまな皮膚疾患がほとんどの場合に治療可能である。しかし副作用もある。ステロイド外用剤長期連用後のリバウンド現象は時々議論されるが、そのメカニズムは判っていない[1]。ステロイド外用剤を数週間健常人ボランティアに用いた過去の研究においては、ステロイド中断後に表皮は一時的に肥厚する[2]。もしもステロイド外用剤が中止後何の影響も残さないのであれば、表皮は単に元の厚さに戻るだけのはずだ。ステロイド外用剤には角化細胞の増殖を抑える作用があり、角化細胞自身にはコルチゾールを産生する能力があるのだから [3]、ステロイド外用剤が長期連用後に角化細胞のコルチゾール合成を損ない、表皮の一時的な肥厚をきたすという仮説が成り立つ。
コルチゾールは受容体に結合することで作用する。Glucocorticoid receptor alpha (GRA) は主なレセプターであり、mineralcorticoid receptor (MCR) が二次的に働くようである [4,5]。 Glucocorticoid receptor beta(GRB)はGRAのデコイであり機能はない。ステロイド外用剤には、コルチゾール産生能を阻害するほかに、GRAとMCRを抑制しGRBを増加させる可能性がある。
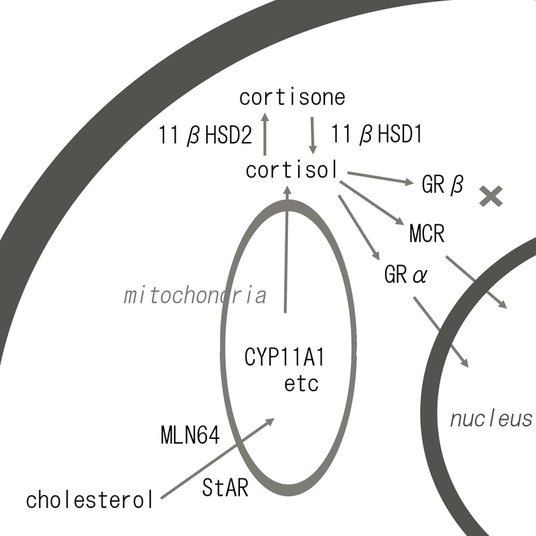
コルチゾールの産生はミトコンドリアへのコレステロールの取り込みで始まる[6]。StAR とMLN64はこの取り込みに必要なタンパク質である。コレステロールはCPY11A1, CPY17, CPY19, CPY21, CPY3B1, HSD3B1 などの様々な酵素によってコルチゾールなどのホルモンへと代謝される。コルチゾールは細胞質内においてHSD11B 2 によって不活性型のコルチゾンに変換され、コルチゾンはHSD11B 1によってコルチゾールへと再活性化される [7]。コルチゾールとその関連物質のイラストをFigure1に示した。
材料と方法
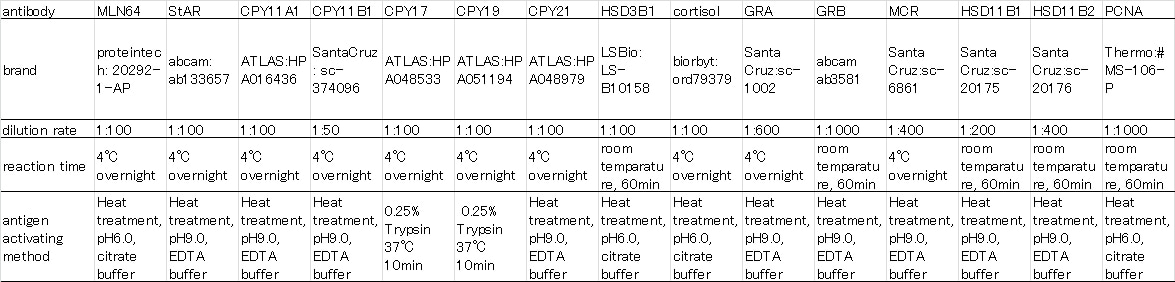
1人の健常人男性(56才)の前腕にclobetasol propionate 0.05%(デルモベート軟膏)を一日二回二週間外用した前後で皮膚を生検した。採取した皮膚をMLN64, StAR, CPY11A1, cortisol, HSD11B1, HSD11B2, GRA, GRB, MCR に対する各種抗体で免疫染色した。染色条件は前もって副腎などの各種臓器の切片を用いて決定した(Table1)。同様の皮膚生検を19人の長期ステロイド外用の経験のある成人アトピー性皮膚炎患者において行った。患者の内訳は、現在ステロイド外用剤使用中(TCS +)が4名、現在ステロイド外用剤を使用しておらず生検部(前腕)に皮疹のある患者(TCS-E+)が12名、ステロイド外用剤を使用しておらず生検部に皮疹がない患者(TCS-E-)が3名である。患者の皮膚は、MLN64, StAR, HSD11B1, HSD11B2, cortisol, GRA, GRB , MCRに対する各種抗体にて染色した。本研究は倫理委員会によって承認されており、すべての患者からインフォームドコンセントを得た。
結果
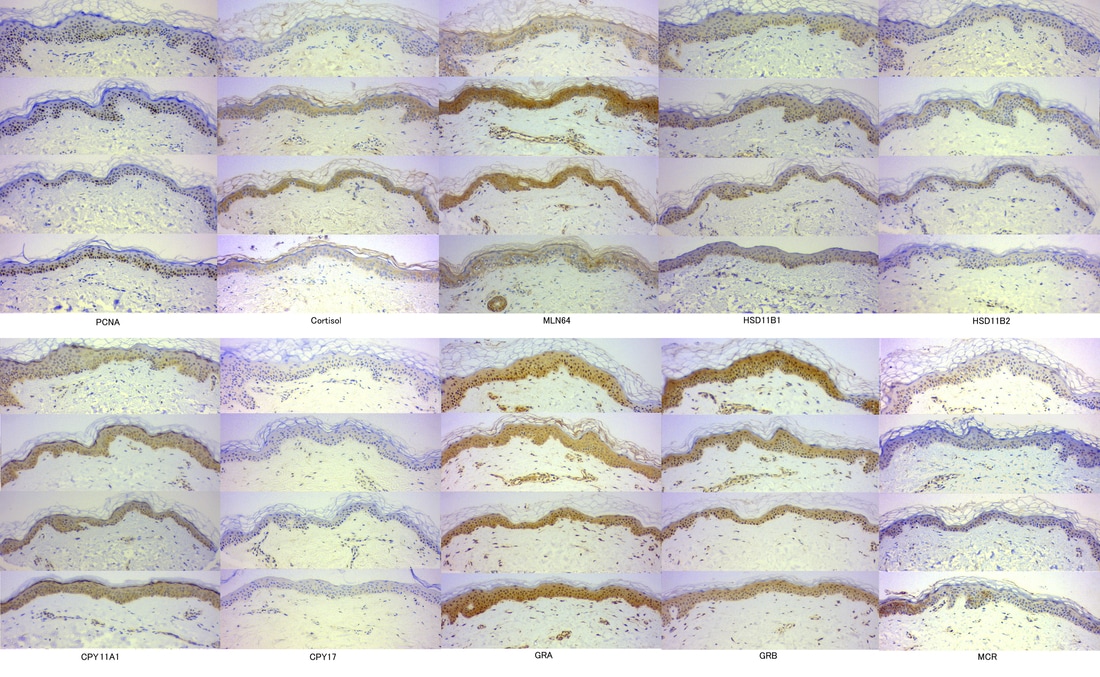
健常者ボランティアでの染色濃度の推移をFigure2に示した。最上段:ステロイド外用前、中上段:ステロイド外用2日後、中下段:ステロイド外用開始から15日後(中止1日後)、最下段: ステロイド外用開始から30日後(中止16日後)。
表皮のコルチゾールは、ステロイド外用後、染色濃度が上昇し、中止後低下した。AtAR, CPY11A1 ほかステロイド合成に関わる酵素はあまり変化がなく、MLN64 はコルチゾールと同様に著明に染色濃度が上昇した。HSD11B2 もまた増強し、MCRはわずかに上昇した。 GRB はステロイド外用後少し染色濃度が低下した。
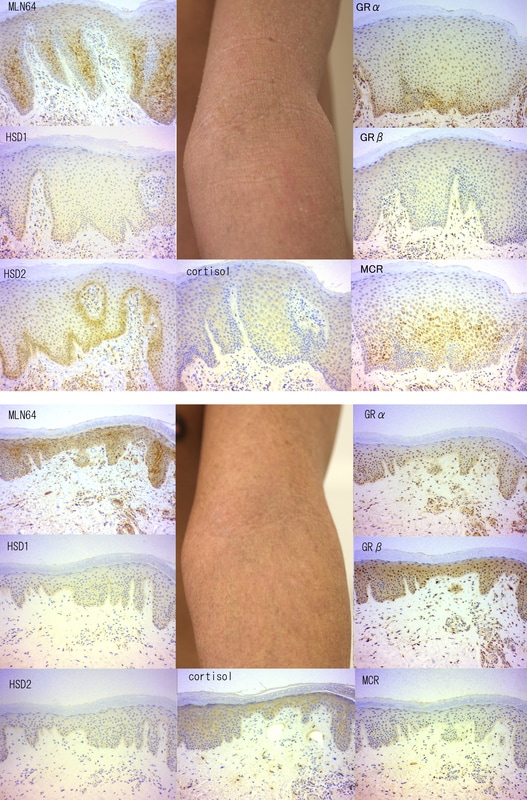
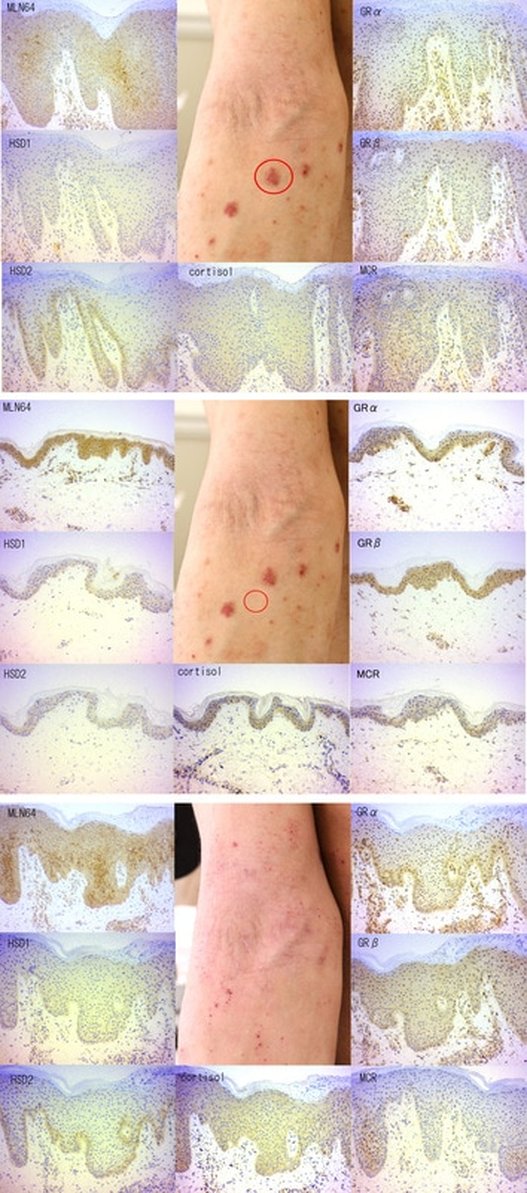
アトピー性皮膚炎患者においては、生検の回数は一回であったが、病態が著明に変化した二人の患者においてのみ二回生検を行った。患者Aにおいてはステロイド外用剤長期連用後のリバウンドの時期に第一回目の生検を行い(Figure 3, 上段)、2年後 リバウンドが落ち着いてきた時期に二回目の生検を行った(Figure 3, 下段)。患者Bはステロイド外用剤を長年使用して以前より効きにくくなったと感じていた。前腕には一見正常な皮膚の中に難治性の湿疹病変が存在していたので、最初の皮膚生検は両部位から採取した(Figure 4, 上段と中段)。患者Bは生検の後、ステロイド外用を中止し、リバウンドを経験した。一か月後、リバウンドがやや治まった後に、二回目の生検を行った (Figure 4, 下段).。
患者Aのリバウンド期には、MLN64 は表皮の中央部でのみ染色されており (有棘層)、HSD11B2 は基底層で著明に染色された。軽快後ではMLN64 は表皮全層で染色されておりHSD11B2 は低下した。軽快後の表皮ではGRB の濃度はより強くなりMCR は消失した。
患者Bにおいては、ステロイド中止前には、一見正常な皮膚において、MLN64 と GRB とが難治性の湿疹部位よりも強く染まっていた。病変部の基底層におけるHSD11B2 も強く染まっていた。ステロイド中止後は、基底層のHSD11B1は、中止前の難治性の湿疹部位と同程度の 濃さであったが、MLN64 は増強していた。
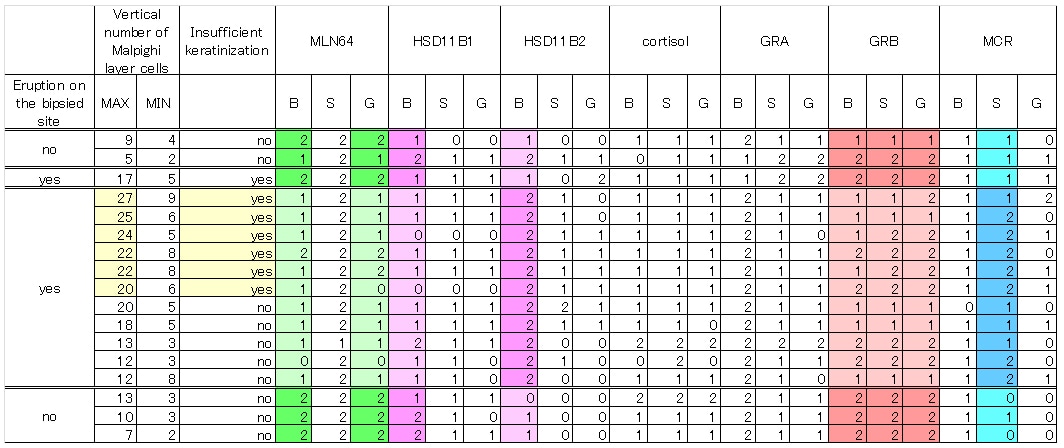
その他の17名の患者の結果をTable 2にまとめた。サンプル数は少ないものの、いくつかの傾向が認められた。すなわち、1)基底層・顆粒層のMLN64は TCS-E+ の患者において弱い (緑色)、2)基底層におけるHSD11B2 染色濃度は、HSD11B1よりも、 TCS-E+ 群において強く、TCS+とTCS-E- 群においてはそれが逆転する (マゼンタ色)、3)TCS-E+群ではGRBは弱い(赤色)、4)TCS-E+群ではMCRは有棘層で強く染色される(青色)。
マルピギー層の細胞の重なり数の最大値(表皮肥厚の指標)はTCS-E+群で明らかに多く、不全角化が表皮の肥厚と一致する点は注目に値する(黄色)。
考察
ステロイド外用によって、表皮のコルチゾール産生が加速するというのは受け入れがたい話ではない。真皮の繊維芽細胞においても同様のステロイド合成の正のフィードバック機構が報告されている[8]。副腎が外界のストレスによってコルチゾールを産生するとき、皮膚は最前線のバリアとしてより多くのコルチゾールを必要とするのだろう。
コルチゾール合成経路の構成要素の中ではMLN64が最も劇的に制御を担っているようだ。他の蛋白質や酵素は健常人ボランティアでのステロイド外用実験で染色濃度の変化を認めなかったので、患者の染色においては省くこととした。健常人においてはHSD11B2 は顆粒層で染色が強かったという報告がある [7]。一方、皮膚腫瘍においては、基底層においてHSD11B2 の染色が強かったという報告もある[9]。アトピー性皮膚炎の場合、特にステロイド長期連用後中止しリバウンドを生じている場合には、HSD11B2 は主に基底層で増強するようである。健常人においてHSD11B2 はステロイド外用によって増強することを考えると、HSD11B2 の増加は過剰なステロイドを不活性化するように働くのだろう。もしもこのメカニズムがステロイド長期外用によって増強され、外用中止後も残るとすれば、表皮はコルチゾール不足に陥り、肥厚と不全角化が引き起こされるだろう。なぜなら表皮においてコルチゾールは増殖と分化の自己調節に働いているからだ。
コルチゾールの染色自体は、患者間で著明には異なっていなかった。著者は、コルチゾールの免疫組織染色の感度の問題だろうと考える。MLN64 とHSD11B2 の変動は大きく、表皮にとって非常に重要なコルチゾールの恒常性を維持すべく働いていると考えられた。レセプターについては、GRA 濃度はあまり変動が無かった。GRBが健常人のステロイド外用後に少し減少するというのは予想外であった。GRBはGRAに拮抗するので、ステロイド外用後には上昇してもよさそうだったからである。GRBはステロイド抵抗性と関係があるとする複数の報告がある。GRBはコルチゾールのシグナルをよりはっきりさせる役割を果たしているのかもしれない。ステロイドが増加した時にGRBが低下すれば、オンオフのスイッチがより明確になるからである。
TCS-E+患者におけるGRB低下は、コルチゾールとGRAとの結合率が高まっているという意味で、コルチゾールシグナルの崩壊を反映していると考えられる。
MCRはコルチゾール濃度が低いときに現れる二次的なレセプターとして知られている。まとめると、TCS-E+ 患者におけるMLN64の低下、HSD11B2の増加、GRB の低下、MCR の増加は、すべてステロイド外用剤長期連用の後遺症であり、コルチゾール恒常性の崩壊を示すものと考えることが出来る。
リバウンド現象、別名Red Skin Syndrome (RSS) [10] または ステロイド外用剤依存[11,12]は、皮膚科領域の悩ましい問題である。それは、患者がアトピー性皮膚炎である場合や、アトピー素因を持つ場合に生じやすい [13]。リバウンドの皮膚症状が原疾患と区別しにくいため、この病態を独立した疾患と認知する医師はまだ少なく、研究もなされていない。本研究がこの病態を紐解く一助になればと思う。
もしも、表皮におけるコルチゾール恒常性の障害がリバウンドの原因であるなら、表皮におけるコルチゾール産生を促すことが患者の回復につながる。UVB療法は、表皮のコルチゾール濃度を高めることが報告されている[14] し、環境の乾燥もまたそうである[15]。RSSの臨床においては、UVBや保湿剤の制限は、いずれも経験的に有用な療法である。タール剤外用は、タールのいくつかの成分がCPY11A1によって代謝されるため、コルチゾール合成を促進させる可能性がある。グリチルリチンはHSD11B2 拮抗剤であり、[16] この薬剤でRSSを治療する医師もいる。
最後に著者は、本研究は症例数が少なく、免疫組織学的手法には定量性が少ないという点を認める。しかし、ステロイド外用剤の後遺症やRSSについての研究は少ないので、本研究は将来のより進んだ研究のための礎となるだろう。
文献
1. Ghosh A, Sengupta S, Coondoo A, Jana AK. Topical corticosteroid addiction and phobia. Indian J Dermatol 2014;59:465-8.
2. Zheng PS, Lavker RM, Lehmann P, Kligman AM. Morphologic investigations on the rebound phenomenon after corticosteroid-induced atrophy in human skin. J Invest Dermatol 1984;82:345-52.
3. Slominski A, Zbytek B, Nikolakis G, Manna PR, Skobowiat C, Zmijewski M, et al. Steroidogenesis in the skin: implications for local immune functions. J Steroid Biochem Mol Biol 2013;137:107-23.
4. Maubec E, Laouénan C, Deschamps L, Nguyen VT, Scheer-Senyarich I, Wackenheim-Jacobs AC et al. Topical Mineralocorticoid Receptor Blockade Limits Glucocorticoid-Induced Epidermal Atrophy in Human Skin. J Invest Dermatol 2015 ;135:1781-9.
5. Boix J, Sevilla LM, Sáez Z, Carceller E, Pérez P. Epidermal Mineralocorticoid Receptor Plays Beneficial and Adverse Effects in Skin and Mediates Glucocorticoid Responses. J Invest Dermatol 2016;136:2417-26.
6. Slominski AT, Manna PR, Tuckey RC. On the role of skin in the regulation of local and systemic steroidogenic activities. Steroids 2015;103:72-88.
7. Cirillo N1, Prime SS. Keratinocytes synthesize and activate cortisol. J Cell Biochem 2011;112:1499-505.
8. Tiganescu A, Walker EA, Hardy RS, Mayes AE, Stewart PM. Localization, age- and site-dependent expression, and regulation of 11β-hydroxysteroid dehydrogenase type 1 in skin. J Invest Dermatol 2011;131:30-6.
9. Terao M, Itoi S, Murota H, Katayama I. Expression profiles of cortisol-inactivating enzyme, 11β-hydroxysteroid dehydrogenase-2, in human epidermal tumors and its role in keratinocyte proliferation. Exp Dermatol 2013;22:98-101.
10. Rapaport MJ, Rapaport V. The red skin syndromes: corticosteroid addiction and withdrawal. Expert Rev Dermatol 2006;1:547-61.
11. Fukaya M, Sato K, Sato M, Kimata H, Fujisawa S, Dozono H et al. Topical steroid addiction in atopic dermatitis. Drug Healthc Patient Saf 2014; 6:131-8.
12. Hajar T, Leshem YA, Hanifin JM, Nedorost ST, Lio PA, Paller AS et al. A systematic review of topical corticosteroid withdrawal ("steroid addiction") in patients with atopic dermatitis and other dermatoses. J Am Acad Dermatol 2015;72:541-9.
13. Kligman AM, Frosch PJ. Steroid addiction. Int J Dermatol. 1979;18:23-31.
14. Tiganescu A, Hupe M, Jiang YJ, Celli A, Uchida Y, Mauro TM. UVB induces epidermal 11β-hydroxysteroid dehydrogenase type 1 activity in vivo. Exp Dermatol. 2015;24:370-6.
15. Takei K, Denda S, Kumamoto J, Denda M. Low environmental humidity induces synthesis and release of cortisol in an epidermal organotypic culture system. Exp Dermatol 2013;22:662-4.
16. Greaves MW. Potentiation of hydrocortisone activity in skin by glycerrhetinic acid. Lancet. 1990;336(8719):876.
Figure 1
コルチゾール合成経路とレセプターのまとめ
先回の6か月調査の論文(→こちら)は、疫学的なものですが、今回は基礎的な面からの研究です。こうして手を替え品を替えてPubmed収載の医学論文として報告していけば、いつかタブーが崩れて、皮膚科医たちが真剣にこの問題を議論する日が来るでしょう。そう信じます。
☆ーーーーー☆ーーーーー☆ーーーーー☆ーーーーー☆
アトピー性皮膚炎患者へのステロイド外用は表皮におけるコルチゾールの恒常性に影響を与える
要約
背景:
皮膚はコルチゾールを産生し自身の増殖・分化を調節している。ステロイド外用剤は皮膚におけるコルチゾールの恒常性に影響を与える可能性がある。
目的と対象:
ステロイド外用後の表皮におけるコルチゾールおよびその関連物質の分布と濃度の免疫組織学的検討。
材料と方法:
1人の健常人男性の前腕にclobetasol propionate 0.05%(デルモベート軟膏)を二週間一日二回外用し、前後で皮膚を生検した。採取した皮膚をMLN64, StAR, CPY11A1, cortisol, HSD11B1, HSD11B2, GRA, GRB, MCR に対する各種抗体で免疫染色した。同様の皮膚生検を19人の長期間ステロイド外用の経験のある成人アトピー性皮膚炎患者において行った。患者の内訳は、現在ステロイド外用剤使用中(TCS +)が4名、現在ステロイド外用剤を使用しておらず生検部(前腕)に皮疹のある患者(TCS-E+)が12名、ステロイド外用剤を使用しておらず生検部に皮疹がない患者(TCS-E-)が3名である。
結果:
健常人ボランティアにおけるMLN64, cortisol, HSD11B2の染色強度はステロイド外用中増加した。TCS-E+ 患者においては、TCS + 患者や TCS-E-患者よりも基底層でHSD11B2が、有棘層でMCR の染色が強かった。またTCS-E+ 患者においては、TCS + 患者や TCS-E-患者よりも基底層と顆粒層でのMLN64染色が弱く、基底層でのHSD11B1 の染色が弱く、全層のGRB の染色が弱かった。
結論:
TCS-E+患者にみられる表皮の肥厚と不全角化は、MLN64によって調節されるコルチゾール合成能の低下と、HSD11B2によるコルチゾールの不活性化によるのかもしれない。GRB の減少とMCR の増加は角化細胞におけるコルチゾールの反応性を高めているのかもしれない。
はじめに
ステロイド外用剤は有用で一般的な皮膚科領域の薬剤であり、さまざまな皮膚疾患がほとんどの場合に治療可能である。しかし副作用もある。ステロイド外用剤長期連用後のリバウンド現象は時々議論されるが、そのメカニズムは判っていない[1]。ステロイド外用剤を数週間健常人ボランティアに用いた過去の研究においては、ステロイド中断後に表皮は一時的に肥厚する[2]。もしもステロイド外用剤が中止後何の影響も残さないのであれば、表皮は単に元の厚さに戻るだけのはずだ。ステロイド外用剤には角化細胞の増殖を抑える作用があり、角化細胞自身にはコルチゾールを産生する能力があるのだから [3]、ステロイド外用剤が長期連用後に角化細胞のコルチゾール合成を損ない、表皮の一時的な肥厚をきたすという仮説が成り立つ。
コルチゾールは受容体に結合することで作用する。Glucocorticoid receptor alpha (GRA) は主なレセプターであり、mineralcorticoid receptor (MCR) が二次的に働くようである [4,5]。 Glucocorticoid receptor beta(GRB)はGRAのデコイであり機能はない。ステロイド外用剤には、コルチゾール産生能を阻害するほかに、GRAとMCRを抑制しGRBを増加させる可能性がある。
コルチゾールの産生はミトコンドリアへのコレステロールの取り込みで始まる[6]。StAR とMLN64はこの取り込みに必要なタンパク質である。コレステロールはCPY11A1, CPY17, CPY19, CPY21, CPY3B1, HSD3B1 などの様々な酵素によってコルチゾールなどのホルモンへと代謝される。コルチゾールは細胞質内においてHSD11B 2 によって不活性型のコルチゾンに変換され、コルチゾンはHSD11B 1によってコルチゾールへと再活性化される [7]。コルチゾールとその関連物質のイラストをFigure1に示した。
材料と方法
1人の健常人男性(56才)の前腕にclobetasol propionate 0.05%(デルモベート軟膏)を一日二回二週間外用した前後で皮膚を生検した。採取した皮膚をMLN64, StAR, CPY11A1, cortisol, HSD11B1, HSD11B2, GRA, GRB, MCR に対する各種抗体で免疫染色した。染色条件は前もって副腎などの各種臓器の切片を用いて決定した(Table1)。同様の皮膚生検を19人の長期ステロイド外用の経験のある成人アトピー性皮膚炎患者において行った。患者の内訳は、現在ステロイド外用剤使用中(TCS +)が4名、現在ステロイド外用剤を使用しておらず生検部(前腕)に皮疹のある患者(TCS-E+)が12名、ステロイド外用剤を使用しておらず生検部に皮疹がない患者(TCS-E-)が3名である。患者の皮膚は、MLN64, StAR, HSD11B1, HSD11B2, cortisol, GRA, GRB , MCRに対する各種抗体にて染色した。本研究は倫理委員会によって承認されており、すべての患者からインフォームドコンセントを得た。
結果
健常者ボランティアでの染色濃度の推移をFigure2に示した。最上段:ステロイド外用前、中上段:ステロイド外用2日後、中下段:ステロイド外用開始から15日後(中止1日後)、最下段: ステロイド外用開始から30日後(中止16日後)。
表皮のコルチゾールは、ステロイド外用後、染色濃度が上昇し、中止後低下した。AtAR, CPY11A1 ほかステロイド合成に関わる酵素はあまり変化がなく、MLN64 はコルチゾールと同様に著明に染色濃度が上昇した。HSD11B2 もまた増強し、MCRはわずかに上昇した。 GRB はステロイド外用後少し染色濃度が低下した。
アトピー性皮膚炎患者においては、生検の回数は一回であったが、病態が著明に変化した二人の患者においてのみ二回生検を行った。患者Aにおいてはステロイド外用剤長期連用後のリバウンドの時期に第一回目の生検を行い(Figure 3, 上段)、2年後 リバウンドが落ち着いてきた時期に二回目の生検を行った(Figure 3, 下段)。患者Bはステロイド外用剤を長年使用して以前より効きにくくなったと感じていた。前腕には一見正常な皮膚の中に難治性の湿疹病変が存在していたので、最初の皮膚生検は両部位から採取した(Figure 4, 上段と中段)。患者Bは生検の後、ステロイド外用を中止し、リバウンドを経験した。一か月後、リバウンドがやや治まった後に、二回目の生検を行った (Figure 4, 下段).。
患者Aのリバウンド期には、MLN64 は表皮の中央部でのみ染色されており (有棘層)、HSD11B2 は基底層で著明に染色された。軽快後ではMLN64 は表皮全層で染色されておりHSD11B2 は低下した。軽快後の表皮ではGRB の濃度はより強くなりMCR は消失した。
患者Bにおいては、ステロイド中止前には、一見正常な皮膚において、MLN64 と GRB とが難治性の湿疹部位よりも強く染まっていた。病変部の基底層におけるHSD11B2 も強く染まっていた。ステロイド中止後は、基底層のHSD11B1は、中止前の難治性の湿疹部位と同程度の 濃さであったが、MLN64 は増強していた。
その他の17名の患者の結果をTable 2にまとめた。サンプル数は少ないものの、いくつかの傾向が認められた。すなわち、1)基底層・顆粒層のMLN64は TCS-E+ の患者において弱い (緑色)、2)基底層におけるHSD11B2 染色濃度は、HSD11B1よりも、 TCS-E+ 群において強く、TCS+とTCS-E- 群においてはそれが逆転する (マゼンタ色)、3)TCS-E+群ではGRBは弱い(赤色)、4)TCS-E+群ではMCRは有棘層で強く染色される(青色)。
マルピギー層の細胞の重なり数の最大値(表皮肥厚の指標)はTCS-E+群で明らかに多く、不全角化が表皮の肥厚と一致する点は注目に値する(黄色)。
考察
ステロイド外用によって、表皮のコルチゾール産生が加速するというのは受け入れがたい話ではない。真皮の繊維芽細胞においても同様のステロイド合成の正のフィードバック機構が報告されている[8]。副腎が外界のストレスによってコルチゾールを産生するとき、皮膚は最前線のバリアとしてより多くのコルチゾールを必要とするのだろう。
コルチゾール合成経路の構成要素の中ではMLN64が最も劇的に制御を担っているようだ。他の蛋白質や酵素は健常人ボランティアでのステロイド外用実験で染色濃度の変化を認めなかったので、患者の染色においては省くこととした。健常人においてはHSD11B2 は顆粒層で染色が強かったという報告がある [7]。一方、皮膚腫瘍においては、基底層においてHSD11B2 の染色が強かったという報告もある[9]。アトピー性皮膚炎の場合、特にステロイド長期連用後中止しリバウンドを生じている場合には、HSD11B2 は主に基底層で増強するようである。健常人においてHSD11B2 はステロイド外用によって増強することを考えると、HSD11B2 の増加は過剰なステロイドを不活性化するように働くのだろう。もしもこのメカニズムがステロイド長期外用によって増強され、外用中止後も残るとすれば、表皮はコルチゾール不足に陥り、肥厚と不全角化が引き起こされるだろう。なぜなら表皮においてコルチゾールは増殖と分化の自己調節に働いているからだ。
コルチゾールの染色自体は、患者間で著明には異なっていなかった。著者は、コルチゾールの免疫組織染色の感度の問題だろうと考える。MLN64 とHSD11B2 の変動は大きく、表皮にとって非常に重要なコルチゾールの恒常性を維持すべく働いていると考えられた。レセプターについては、GRA 濃度はあまり変動が無かった。GRBが健常人のステロイド外用後に少し減少するというのは予想外であった。GRBはGRAに拮抗するので、ステロイド外用後には上昇してもよさそうだったからである。GRBはステロイド抵抗性と関係があるとする複数の報告がある。GRBはコルチゾールのシグナルをよりはっきりさせる役割を果たしているのかもしれない。ステロイドが増加した時にGRBが低下すれば、オンオフのスイッチがより明確になるからである。
TCS-E+患者におけるGRB低下は、コルチゾールとGRAとの結合率が高まっているという意味で、コルチゾールシグナルの崩壊を反映していると考えられる。
MCRはコルチゾール濃度が低いときに現れる二次的なレセプターとして知られている。まとめると、TCS-E+ 患者におけるMLN64の低下、HSD11B2の増加、GRB の低下、MCR の増加は、すべてステロイド外用剤長期連用の後遺症であり、コルチゾール恒常性の崩壊を示すものと考えることが出来る。
リバウンド現象、別名Red Skin Syndrome (RSS) [10] または ステロイド外用剤依存[11,12]は、皮膚科領域の悩ましい問題である。それは、患者がアトピー性皮膚炎である場合や、アトピー素因を持つ場合に生じやすい [13]。リバウンドの皮膚症状が原疾患と区別しにくいため、この病態を独立した疾患と認知する医師はまだ少なく、研究もなされていない。本研究がこの病態を紐解く一助になればと思う。
もしも、表皮におけるコルチゾール恒常性の障害がリバウンドの原因であるなら、表皮におけるコルチゾール産生を促すことが患者の回復につながる。UVB療法は、表皮のコルチゾール濃度を高めることが報告されている[14] し、環境の乾燥もまたそうである[15]。RSSの臨床においては、UVBや保湿剤の制限は、いずれも経験的に有用な療法である。タール剤外用は、タールのいくつかの成分がCPY11A1によって代謝されるため、コルチゾール合成を促進させる可能性がある。グリチルリチンはHSD11B2 拮抗剤であり、[16] この薬剤でRSSを治療する医師もいる。
最後に著者は、本研究は症例数が少なく、免疫組織学的手法には定量性が少ないという点を認める。しかし、ステロイド外用剤の後遺症やRSSについての研究は少ないので、本研究は将来のより進んだ研究のための礎となるだろう。
文献
1. Ghosh A, Sengupta S, Coondoo A, Jana AK. Topical corticosteroid addiction and phobia. Indian J Dermatol 2014;59:465-8.
2. Zheng PS, Lavker RM, Lehmann P, Kligman AM. Morphologic investigations on the rebound phenomenon after corticosteroid-induced atrophy in human skin. J Invest Dermatol 1984;82:345-52.
3. Slominski A, Zbytek B, Nikolakis G, Manna PR, Skobowiat C, Zmijewski M, et al. Steroidogenesis in the skin: implications for local immune functions. J Steroid Biochem Mol Biol 2013;137:107-23.
4. Maubec E, Laouénan C, Deschamps L, Nguyen VT, Scheer-Senyarich I, Wackenheim-Jacobs AC et al. Topical Mineralocorticoid Receptor Blockade Limits Glucocorticoid-Induced Epidermal Atrophy in Human Skin. J Invest Dermatol 2015 ;135:1781-9.
5. Boix J, Sevilla LM, Sáez Z, Carceller E, Pérez P. Epidermal Mineralocorticoid Receptor Plays Beneficial and Adverse Effects in Skin and Mediates Glucocorticoid Responses. J Invest Dermatol 2016;136:2417-26.
6. Slominski AT, Manna PR, Tuckey RC. On the role of skin in the regulation of local and systemic steroidogenic activities. Steroids 2015;103:72-88.
7. Cirillo N1, Prime SS. Keratinocytes synthesize and activate cortisol. J Cell Biochem 2011;112:1499-505.
8. Tiganescu A, Walker EA, Hardy RS, Mayes AE, Stewart PM. Localization, age- and site-dependent expression, and regulation of 11β-hydroxysteroid dehydrogenase type 1 in skin. J Invest Dermatol 2011;131:30-6.
9. Terao M, Itoi S, Murota H, Katayama I. Expression profiles of cortisol-inactivating enzyme, 11β-hydroxysteroid dehydrogenase-2, in human epidermal tumors and its role in keratinocyte proliferation. Exp Dermatol 2013;22:98-101.
10. Rapaport MJ, Rapaport V. The red skin syndromes: corticosteroid addiction and withdrawal. Expert Rev Dermatol 2006;1:547-61.
11. Fukaya M, Sato K, Sato M, Kimata H, Fujisawa S, Dozono H et al. Topical steroid addiction in atopic dermatitis. Drug Healthc Patient Saf 2014; 6:131-8.
12. Hajar T, Leshem YA, Hanifin JM, Nedorost ST, Lio PA, Paller AS et al. A systematic review of topical corticosteroid withdrawal ("steroid addiction") in patients with atopic dermatitis and other dermatoses. J Am Acad Dermatol 2015;72:541-9.
13. Kligman AM, Frosch PJ. Steroid addiction. Int J Dermatol. 1979;18:23-31.
14. Tiganescu A, Hupe M, Jiang YJ, Celli A, Uchida Y, Mauro TM. UVB induces epidermal 11β-hydroxysteroid dehydrogenase type 1 activity in vivo. Exp Dermatol. 2015;24:370-6.
15. Takei K, Denda S, Kumamoto J, Denda M. Low environmental humidity induces synthesis and release of cortisol in an epidermal organotypic culture system. Exp Dermatol 2013;22:662-4.
16. Greaves MW. Potentiation of hydrocortisone activity in skin by glycerrhetinic acid. Lancet. 1990;336(8719):876.
Figure 1
コルチゾール合成経路とレセプターのまとめ
Figure2
健常人ボランティアのPCNA, cortisol, MLN64, HSD11B1, HSD11B2, CPY11A1, CPY17, GRA, GRB, MCR 各種抗体を用いた免疫組織染色
健常人ボランティアのPCNA, cortisol, MLN64, HSD11B1, HSD11B2, CPY11A1, CPY17, GRA, GRB, MCR 各種抗体を用いた免疫組織染色
Figure 3
患者Aの臨床像とMLN64, HSD11B1, HSD11B2, cortisol, GRA, GRB, MCRによる免疫組織染色結果
患者Aの臨床像とMLN64, HSD11B1, HSD11B2, cortisol, GRA, GRB, MCRによる免疫組織染色結果
Figure 4
患者Bの臨床像とMLN64, HSD11B1, HSD11B2, cortisol, GRA, GRB, MCRによる免疫組織染色結果
患者Bの臨床像とMLN64, HSD11B1, HSD11B2, cortisol, GRA, GRB, MCRによる免疫組織染色結果
Table1
各種抗体の免疫組織染色条件
各種抗体の免疫組織染色条件
Table2
17名の患者の免疫組織学的染色のまとめ。B; 基底層S; 有棘層, G; 顆粒層。0; 認めず、または軽微, 1; 中程度, 2; 強度。
17名の患者の免疫組織学的染色のまとめ。B; 基底層S; 有棘層, G; 顆粒層。0; 認めず、または軽微, 1; 中程度, 2; 強度。
私が作製した中間分子量ヒアルロン酸化粧水「ヒアルプロテクト」のショップはこちら(下の画像をクリック)